Сияющие акценты: Как использовать неоновые вывески из гибкого неона "neon-show" для оригинального дизайна интерьера
Апрель 15, 2024 – 22:38В последние годы неоновые вывески вновь обрели популярность как модный и привлекающий внимание элемент дизайна интерьера. Однако традиционные неоновые вывески имеют такие недостатки, как хрупкость и высокое энергопотребление...
Краткая биографическая справка о Брежневе и Зачем знание истории необходимо для современного человека
Апрель 12, 2024 – 17:54Леонид Ильич Брежнев (1906–1982) – советский политик, который занимал пост Генерального секретаря ЦК КПСС с 1964 по 1982 год. В своей долгой политической карьере он играл ключевую роль в формировании советской внутренней...
Маленькие радости: Почему дарение сувениров является приятной традицией и приносит удовольствие как дарителю, так и получателю
Апрель 12, 2024 – 13:17Дарить подарки - это вечная традиция, которая охватывает все культуры, случаи жизни и отношения. От дней рождения и праздников до свадеб и торжеств - акт дарения и получения подарков приносит в нашу жизнь радость...
Уплотнение грунта и асфальта: Руководство по выбору и использованию виброплит для строительства и дорожных работ
Апрель 12, 2024 – 13:05Уплотнение грунта и асфальта - важнейшие процессы в строительстве и дорожных работах, обеспечивающие стабильность, прочность и долговечность инфраструктуры. Виброплиты , также известные как пластинчатые катки или...
Забудьте о сигаретах: Почему переход на вейп может быть отличной альтернативой курению
Апрель 11, 2024 – 17:18Для многих людей решение бросить курить сигареты является важным шагом на пути к улучшению здоровья и самочувствия. Хотя бросить курить с холодной индейкой может быть непросто, переход на вейпинг предлагает многообещающую...
Cтильные и функциональные решения: Производство и установка дверей невидимки и зеркальных дверей для вашего интерьера
Апрель 4, 2024 – 13:00В современном дизайне первостепенное значение имеет органичное сочетание функциональности и эстетики. Невидимые и зеркальные двери предлагают инновационные решения для интерьера, обеспечивая как практичность, так...
Идеальный спутник: Как выбрать планшет, который подходит именно вам
Март 20, 2024 – 18:05В современный цифровой век планшеты стали незаменимыми спутниками как на работе, так и на отдыхе. При огромном количестве вариантов, представленных на рынке, выбор подходящего планшета может стать непростой задачей...
От офлайн к онлайн: Рассматриваем плюсы и минусы различных форм обучения и выбираем оптимальный путь для успешного обучения ребенка
Март 15, 2024 – 12:46В современную цифровую эпоху сфера образования претерпела значительные изменения: традиционное офлайн-обучение теперь делит свет с инновационными онлайн-альтернативами. Родителям, ориентирующимся в огромном количестве...
Откройте потенциал: Как развить интуицию и скрытые способности у женщин
Март 11, 2024 – 13:17В современном быстро меняющемся мире невозможно переоценить важность женской интуиции и скрытых способностей. Эти врожденные качества, которые часто игнорируются или недооцениваются, обладают огромным потенциалом...
Мастерство в Интернете: Почему WebValley Studio Считается Лучшими в Области Разработки и Продвижения Сайтов
Ноябрь 25, 2023 – 12:36В условиях постоянно расширяющегося цифрового ландшафта успех любого бизнеса часто зависит от сильного присутствия в Интернете, и студия WebValley стала одним из ключевых игроков в области разработки и продвижения...
Оставьте Ржавчине Шанс: Лучшие Средства для Борьбы с Коррозией в Сантехнике
Декабрь 6, 2023 – 10:15В запутанной сети труб, пронизывающих наши дома и здания, коррозия предстает грозным противником, молчаливо угрожающим целостности водопроводных систем. Однако с развитием средств борьбы с коррозией пришло время...
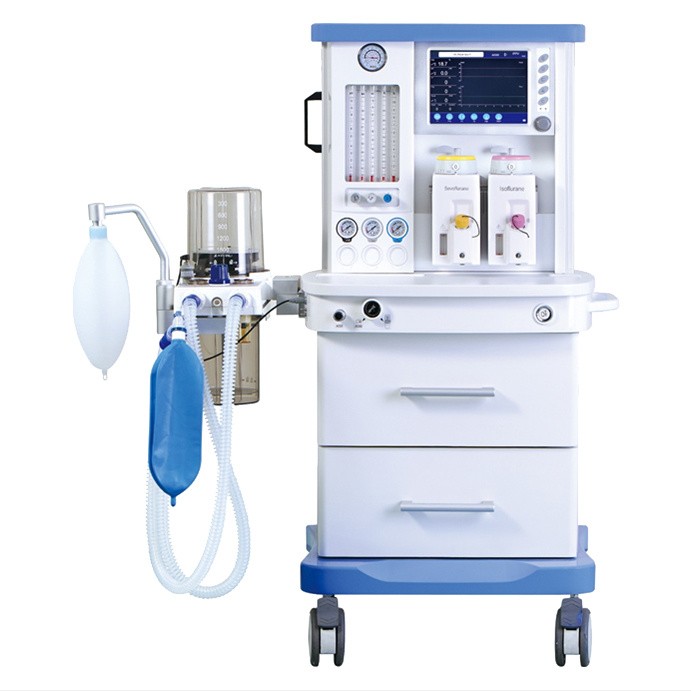
Технологии для комфорта: Как наркозно-дыхательные аппараты обеспечивают безопасный наркоз и вентиляцию
Октябрь 31, 2023 – 12:17В области здравоохранения разработка и использование передовых технологий позволили значительно повысить комфорт и безопасность пациентов при проведении хирургических операций. Анестезиологические и дыхательные...
Аварийный комиссар ДТП: роль и обязанности в процессе разбирательства дорожно-транспортного происшествия
Октябрь 18, 2023 – 15:58Во многих правовых системах комиссар по ДТП играет важную роль в контроле и управлении процессом рассмотрения дорожно-транспортных происшествий. В его обязанности входят различные аспекты расследования ДТП и обеспечение...
Оптимизация процессов и ресурсов: Как менеджмент способствует повышению эффективности в строительной отрасли
Июль 19, 2023 – 13:25Строительная отрасль известна своей сложностью, разнообразием заинтересованных сторон и необходимостью управлять множеством процессов одновременно. На сайте https://moscow.mba/programs/mba/online/construction-management...
Изысканный отдых: почему номера люкс считаются лучшим вариантом всех времен
Август 13, 2023 – 12:12Изысканный отдых часто предполагает проживание в роскошных номерах, обеспечивающих комфорт, уединение и исключительное обслуживание. Рекомендуем посетить шикарный номер люкс в отеле Grace Calipso, яркие впечатления...
Порядок и требования: как узаконить перепланировку в соответствии с законодательством
Июль 10, 2023 – 09:26Проекты редевелопмента открывают возможности для преобразования существующих объектов недвижимости и максимального раскрытия их потенциала. Однако во избежание юридических проблем и штрафов необходимо убедиться...
s-zametki.ru ,
порно секс ,
Новое порно ,
https://www.juristi-helsinki.eu ,
https://www.comment-enlever.fr/ ,
https://lakitoimistovantaa.net/ ,
https://reussirsaboutiqueenligne.fr/ ,
ххх видео подростки ,
https://lakiasiaintoimisto-vantaa.com/ ,
https://www.lakiasiaintoimisto-espoo.fi/ ,
девушки по вызову секс стерлитамак ,
Описание дорогие проститутки калуга у нас. ,
Проститутки балашихи снять девочку по вызову в балашихе. ,
Подробная информация проверенные индивидуалки калуги у нас. ,
Верфь Velvette Marine https://velvette-marine.com/ официальный сайт производителя.